|
|
|
|
Международный проект по ликвидации СОЗ
Поощрение активного и эффективного участия участия гражданского общества в подготовке к выполнению Стокгольмской конвенции
ОТЧЕТ по проекту «ДДТ и ДДЕ в Российской Арктике и репродуктивное здоровье коренного населения»
Координатор – Алексей Дударев
Северо-Западный научный центр гигиены и общественного здоровья
Электронная почта: dudarev @ sp . ru
Содержание
1. Введение |
2. Описание проекта |
Цели и задачи |
3. Материалы и методы |
3.1. Объекты исследований |
3.2. География исследований и группы наблюдения |
3.3. ДДТ и его метаболиты, рассматриваемые в проекте |
3.4 Методы отбора проб крови. Хранение, транспортировка |
3.5. Аналитические методы и контроль качества |
3.6. Анкетирование и методика опроса |
3.7. Методы статистического и эпидемиологического анализа |
4. Результаты и обсуждение |
4.1. Содержание ДДТ и его метаболитов в крови родильниц |
4.2. Репродуктивное здоровье в связи с воздействием ДДТ и его метаболитов |
4.2.1. Неблагоприятные исходы беременности |
4.2.2. Репродуктивный анамнез родильниц |
4.2.3. Соотношение полов новорожденных детей |
5. Выводы |
Использованные сокращения:
ДДТ – дихлордифенилтрихлорэтан (1,1,1–трихлор-2,2,-бис(р-хлорфенил)этан).
2,4 ДДТ; 4,4 ДДТ; 2,4 ДДЕ; 4,4 ДДЕ; 2,4 ДДД; 4,4 ДДД – метаболиты ДДТ.
n – число наблюдений.
p – value – статистическая достоверность различий сравниваемых совокупностей.
r – коэффициент корреляции.
RR ( relative risk ) – относительный риск
НАО – Ненецкий автономный округ.
ТАО – Таймырский автономный округ.
ЧАО – Чукотский автономный округ.
ВПР – врожденные пороки развития.
НИБ – неблагоприятные исходы беременности.
Данный проект был осуществлен при финансовой поддержке Центра «Эко-Согласие» на основе совокупных материалов и информации , собранных в ходе реализации нескольких проектов. Крупномасштабный GEF/AMAP/RAIPON проект « Стойкие токсичные вещества , безопасность питания и коренные народы Российского Севера » 2000-2004 гг . явился основой (на 2/3) материалов баз данных, использованных в данном проекте; дополнительные 30% информации были получены позже.
Выражаем благодарность за участие в сборе первичной информации (анкетных данных), получении проб крови и в целом за помощь в осуществлении проекта персоналу родильных отделений областных, окружных и районных больниц Мурманской области, Ненецкого, Таймырского и Чукотского автономных округов.
Мы признательны за предварительную подготовку и помощь в организации работ на местах сотрудникам Администраций, Управлений Здравоохранения и центрам санитарно-эпидемиологического надзора Мурманской области, Ненецкого, Таймырского и Чукотского автономных округов.
Отдельную благодарность выражаем Институту Общественной Медицины (г. Тромсё, Норвегия) за выполнение химического анализа части проб крови.
Введение
Первые в РФ широкомасштабные научные исследования, проведенные с участием СЗНЦГиОЗ в 2001-2005 годах в Арктических районах РФ, позволили установить, что уровни загрязнения объектов окружающей среды стойкими токсическими веществами (СТВ), в том числе ДДТ в основных районах проживания коренных народов Крайнего Севера России (Мурманская область, Ненецкий, Таймырский и Чукотский автономные округа), значительны и сопоставимы с аналогичными уровнями загрязнения в других районах Арктики (Гренландия, Аляска, Канада).
В ходе исследований выявлены значительные концентрации ДДТ в персональных пробах крови коренных жителей Арктики, что свидетельствует о повышенном поступлении этих СТВ в организм аборигенов Крайнего Севера России в связи с загрязнением среды их обитания и традиционной пищи.
Установлено, что основными источниками поступления избыточных количеств ДДТ в организм аборигенов Арктики является употребление в пищу загрязненной рыбы, морских животных и в некоторых случаях дичи. Источниками загрязнения пищи является как глобальный перенос, так и местные источники, приводящие к вторичному загрязнению продуктов питания в процессах их хранения и кулинарной обработки.
Впервые установлено, что во всех районах значительный риск вредного воздействия ДДТ на организм связан (в том числе) с интенсивным загрязнением внутренней среды жилых и общественных зданий (в основном, за счет неконтролируемого применения бытовых инсектицидов), 100% которых по результатам специального выборочного обследования, оказались загрязненными ДДТ.
Традиционная пища коренных народов, проживающих в Российской Арктике, не может считаться безопасной. Как свидетельствуют расчетные данные, основанные на химическом анализе содержания ДДТ в сотнях проб традиционных продуктов питания, удельное поступление ДДТ в организм взрослого человека (в расчете на 1 кг массы тела) за счет употребления основных видов рыбы, мяса, жира и внутренних органов животных, зачастую превышает рекомендованные предельно допустимые значения.
В ходе исследований выявлены значительные уровни содержания СТВ в крови у беременных женщин коренных национальностей Крайнего Севера РФ, концентрации отдельных высокотоксичных веществ (в т.ч. ДДТ) во многих случаях существенно превышали рекомендуемые ВОЗ пределы. Особенностями вредных эффектов, вызываемых ДДТ, является их способность нарушать репродуктивные функции и оказывать неблагоприятное влияние на развитие плода (ATSDR, 2002). Выраженные концентрации в крови ДДТ вызывают изменения в нейроэндокринной, иммунной системах. Некоторые вредные вещества являются “гормональными имитаторами”, подавляя выработку гормонов в организме и нарушая нормальное течение процессов, регулируемых эндокринными железами, таких, как сперматогенез, овуляция и половое развитие. По причине того, что ДДТ растворимы в жире, они легко переносятся через плацентарный барьер, интенсивно поступая в организм ребенка в период внутриутробного развития с кровью матери, и в грудном возрасте - с материнским молоком.
2. Описание проекта
Цели и задачи проекта
Целью проекта является оценка возможных специфических эффектов воздействия ДДТ и его метаболитов на репродуктивное здоровье коренных жителей Российской Арктики.
Задачи проекта:
Используя расширенную базу данных (346 родильниц) – анкеты, содержащие персональные данные о здоровье женщин, их репродуктивном анамнезе, здоровье новорожденных, а также персональные концентрации ДДТ и его метаболитов в материнской крови, проанализировать:
• менструальный статус (возраст начала месячных, продолжительность кровотечений, длительность менструального цикла, интенсивность спазмов и болей при месячных);
• неблагоприятные исходы беременностей (преждевременные роды, выкидыши, мертворождения, эктопические беременности);
• патологию плода (низкий вес новорожденных, врожденные пороки развития);
• соотношение полов новорожденных детей;
• возможные связи и дозовые зависимости менструального статуса, неблагоприятных исходов беременностей, патологии плода, соотношение полов новорожденных с концентрациями в крови матерей ДДТ и его метаболитов;
3. Материалы и методы.
3.1. Объекты исследований.
Объектами исследований являлись беременные женщины коренных национальностей, постоянно проживающие в заполярных и приполярных областях Крайнего Севера России.
3.2. География исследований и группы наблюдения.
Для проведения основных исследований по ДДТ были выбраны 4 района (откуда поступали беременные женщины коренных национальностей):
-
Кольский полуостров (Мурманская область). Район исследований охватывал поселок Ловозеро, основное место компактного проживания саамов, а также поселок Краснощелье.
-
Нижнее течение реки Печоры (Ненецкий АО), заселенное в основном ненцами. Исследования проводились в г. Нарьян-Мар, куда поступали беременные из различных поселков - Нельмин Нос, Индига и др.
-
Полуостров Таймыр (Таймырский или Долгано-Ненецкий АО). Исследования проводились в г. Дудинка (основное коренное население района - ненцы) и п. Хатанга (основное население района - долганы).
-
Чукотский полуостров (Чукотский АО). Было выделено два района проведения исследований, значительно отличающихся друг от друга по образу жизни коренного населения: континентальный Анадырский район - место проживания континентальных чукчей-оленеводов, и прибрежный район северо-восточной Чукотки – место проживания эскимосов и береговых чукчей, исторически занимающихся охотой на морзверя.
В проведении исследования приняли участие беременные женщины коренных национальностей, поступившие в 2001-2002 гг в родильные отделения больниц г. Оленегорск (Мурманская область), г. Нарьян-Мар (НАО), г. Дудинка и пос. Хатанга (ТАО), г. Анадырь, пос. Угольные Копи и пос. Лаврентия (ЧАО). Несколько женщин прошли обследование на Камчатке в родильном отделении областной больницы Петропавловска-Камчатского. В качестве контрольных групп аналогичные исследования выполнены с участием беременных женщин г. Норильск (ТАО) и г. Ургенч (экологически кризисная зона Аральского моря, Узбекистан).
В районах проведения исследований находятся 117 населенных пунктов, где проживает коренное население. Этнический состав населения этих поселков, несмотря на относительно невысокую численность, представляет практически 2/3 общего национального состава коренного населения российской Арктики. Таким образом, районы, выбранные для исследований, позволили получить достаточно представительную (для Российского севера в целом) выборку основных этногенетических групп, характеризующихся исторически сложившимися на данных территориях традиционным образом жизни, рационами питания, особенностями ведения хозяйства, социальным и культурным укладом.
Для оценки содержания ДДТ в организме аборигенов Арктики использовалась кровь беременных женщин и пуповинная кровь новорожденных. Одновременно с отбором проб крови, было проведено детальное анкетирование всех участниц обследования.
Таблица 1.
Число собранных анкет и проанализированных проб крови матерей:
Район обследования |
n |
Мурманская область |
16 |
Ненецкий АО (НАО) |
38 |
Таймырский АО (ТАО) |
69 |
Чукотский АО (ЧАО) – прибрежные районы |
59 |
Чукотский АО (ЧАО) – континентальные районы |
67 |
Камчатка |
8 |
Норильск (ТАО) |
59 |
Ургенч (Арал) |
30 |
Всего |
346 |
3.3. ДДТ и его метаболиты, рассматриваемые в проекте
2,4 ДДТ, 4,4 ДДТ, 2,4 ДДЕ, 4,4 ДДЕ, 2,4 ДДД, 4,4 ДДД, а также сумма ДДТ анализировались в крови беременных женщин.
3.4. Методы отбора проб крови. Хранение, транспортировка.
Для отбора проб крови использовались изделия, специально проверенные на отсутствие примесей устойчивой хлорорганики, включая ДДТ:
Наименование |
Производитель |
Vacutainer 10 mL lavender (BD366457; K 3 EDTA)
for Organochlorines |
Becton Dickinson Vacutainer System (USA) |
Vacutainer Brand Holder Portable-tube |
Becton Dickinson Vacutainer System (USA) |
Needles Vacutainer Sterile |
Becton Dickinson Vacutainer System (USA) |
7 mL Clear Vial, screw cap
for storage of plasma/serum (for Organochlorines) |
Supelco ( USA ) |
Transfer pipettes 3,5 ml № 86.1172.001
for transfer of plasma/serum |
Sarstedt ( Germany ) |
Методика отбора крови у матери и плода
Отбор крови у матери производится из локтевой вены, у плода – из пуповины в несколько этапов последовательно. Отбор крови проводится с помощью вакутайнеров - беспоршневых вакуумных стекло пластиковых пробирок с навинчиваемой (на держатель) иглой для дозированного внутривенного забора крови. Дальнейшая обработка крови требует наличия специальных пипеток и емкостей, проверенных на отсутствие веществ, способных исказить результаты анализов крови. Обработка отобранной крови требует наличия центрифуги мощностью 3000 оборотов/минуту. Хранение крови требует использования морозильной камеры, поддерживающей температуру не выше –20 0 С. Транспортировка замороженной крови осуществляется в специальных термоконтейнерах, исключающих размораживание образцов.
Отбор крови у матери из вены производится на 1-3 день после родов. Отбор крови из пуповины производится при родах сразу после пережима (перевязки) и отсечения пуповины. Методика отбора и обработки материнской крови идентична таковой для пуповинной.
Все используемые для отбора крови инструменты – одноразовые.
Комплект для отбора крови включает:
• 1 держатель иглы
• 1 игла
• 3 вакутайнера (6; 7 и 10 мл)
• 2 пластиковых пузырька с закручивающейся пробкой
• 2 пластиковых пипетки
• 5 наклеек
3.5. Аналитические методы и контроль качества.
Определение ДДТ в пробах крови производилось в НПО «Тайфун» (г. Обнинск, Калужская область), Региональном Центре «Мониторинг Арктики» (Санкт-Петербург), Юнилаб Анализ АС (г. Тромсё, Норвегия) и в Центре Токсикологии (г. Квебек, Канада).
Количественный анализ ДДТ проводился методом газовой хроматографии с регистрацией детектором по захвату электронов ( ECD ). Дополнительно проводился анализ методом GC - MC образцов с аномальным составом поллютантов или их аномально высокими концентрациями для подтверждения наличия определяемых веществ. Для анализа использовался тот же очищенный экстракт, что и при выполнении измерений методом GC - ECD .
Все использованные растворители очищали дополнительной перегонкой. Все использованные для анализа газы имели чистоту не менее 5-0. Все использованные для калибровки стандартные растворы ДДТ – производства Promochem сертифицированы ISO 9001.
Все 4 лаборатории – участницы проекта подтверждали высокое качество аналитических работ при тестировании образцов в рамках международных ринг-тестов, в том числе под эгидой АМАП.
3.6. Анкетирование и методики опроса.
Опрос и отбор крови у беременных женщин (с одновременным отбором пуповинной крови плода) крайне важен с позиций охвата «группы риска».
Анкетирование беременных женщин коренных национальностей в родильных отделениях больниц проводилось медицинским персоналом, прошедшим специальное обучение. Анкеты содержали сведения о национальности, бытовых условиях, семейном положении, работе, доходах, питании (прежде всего, традиционном), вредных привычках, применении инсектицидов, охоте, рыбалке, а также о здоровье. Анкеты также содержали разделы, посвященные репродуктивному анамнезу женщин (исходы беременностей, параметры новорожденных детей, особенности менструального цикла, история болезней) и дублированные сведения из карт новорожденных.
3.7. Методы статистического и эпидемиологического анализа.
Статистическая обработка полученных эпидемиологических данных проводилась по общепринятым методикам.
Полученные результаты регистрировали в компьютерной базе данных. Статистическая обработка фактического материала выполнена с применением программы Microsoft Excel 2003, а также при помощи пакетов прикладных программ SPSS с использованием параметрических и непараметрических методов статистики, корреляционного (коэффициенты Пирсона, Спирмена) и регрессионного анализа, критериев достоверности t Стьюдента, Mann-Whitney.
Для оценки роли конкретных факторов риска использованы принципы эпидемиологической статистики. Для расчета рисков использован метод вычисления коэффициента относительного риска ( RR , relative risk) по Mantel - Haensel и его 95% доверительного интервала с применением 4-х польной таблицы для исследований «случай-контроль» и теста ?2.
4. Результаты и обсуждение.
В отчете будут представлены результаты химического анализа ДДТ в крови матерей и дальнейшего анализа эффектов воздействия ДДТ на организм матери и плода, основанные только на крови матерей. Все анализируемые эффекты, включая вес новорожденных, сопряжены со здоровьем матерей, пуповинная кровь новорожденных не позволила бы проанализировать эффекты воздействия ДДТ на организм матери. Кроме того, подтверждена тесная корреляция содержания ДДТ в организме матери и плода, т.к. плацентарный барьер не способен задерживать ДДТ.
• Содержание ДДТ и его метаболитов в крови родильниц.
Географические отличия содержания ДДТ в крови родильниц представлены в Таблице 2.
Таблица 2.
Концентрации ДДТ и его метаболитов в материнской крови по регионам (мкг/л)
мкг/л |
|
ЧАО конт. |
ЧАО прибр. |
Мурм. обл. |
НАО |
ТАО |
Норильск |
Арал |
Камчатка |
Всего |
n |
67 |
59 |
16 |
38 |
69 |
59 |
30 |
8 |
346 |
2,4 ДДЕ |
ср.геом. |
0,001 |
0,003 |
0,001 |
0,002 |
0,003 |
0,033 |
0,002 |
0,010 |
0,003 |
max |
0,040 |
0,090 |
0,001 |
0,147 |
0,210 |
0,222 |
0,017 |
0,010 |
0,222 |
4,4 ДДЕ |
ср.геом. |
1,425 |
2,411 |
2,059 |
1,589 |
1,497 |
3,164 |
7,792 |
1,745 |
2,161 |
max |
6,350 |
6,980 |
6,559 |
5,440 |
7,650 |
19,645 |
20,762 |
2,453 |
20,762 |
2,4 ДДД |
ср.геом. |
0,001 |
0,001 |
0,001 |
0,001 |
0,001 |
0,009 |
0,002 |
0,010 |
0,003 |
max |
0,001 |
0,001 |
0,001 |
0,001 |
0,001 |
0,321 |
0,080 |
0,010 |
0,321 |
4,4 ДДД |
ср.геом. |
0,008 |
0,010 |
0,007 |
0,005 |
0,004 |
0,002 |
0,008 |
0,013 |
0,007 |
max |
0,178 |
0,302 |
0,102 |
0,140 |
0,182 |
0,040 |
0,500 |
0,021 |
0,500 |
2,4 ДДТ |
ср.геом. |
0,006 |
0,004 |
0,006 |
0,003 |
0,004 |
0,002 |
0,004 |
0,010 |
0,005 |
max |
0,541 |
0,184 |
0,055 |
0,750 |
0,235 |
0,360 |
0,028 |
0,010 |
0,750 |
4,4 ДДТ |
ср.геом. |
0,203 |
0,209 |
0,250 |
0,241 |
0,186 |
0,334 |
0,220 |
0,058 |
0,220 |
max |
1,090 |
1,200 |
0,801 |
1,850 |
0,850 |
6,267 |
3,660 |
0,339 |
6,267 |
? ДДТ |
ср.геом. |
1,702 |
2,732 |
2,365 |
1,929 |
1,779 |
3,690 |
8,212 |
1,887 |
2,512 |
max |
7,115 |
8,052 |
7,517 |
7,377 |
8,019 |
25,911 |
21,407 |
2,488 |
25,911 |
 - наиболее высокие концентрации. - наиболее высокие концентрации.
Максимальные персональные концентрации суммы ДДТ для изучаемых регионов достигали 8 мкг/л плазмы крови у родильниц коренных национальностей Российской Арктики, 26 мкг/л – у родильниц г. Норильск. При этом, вблизи г. Ургенч (приаральская зона экологического неблагополучия по пестицидам в Узбекистане) сумма ДДТ достигала 21 мкг/л плазмы крови родильниц-узбечек, что подтверждает явное присутствие местных источников ДДТ на Севере.
Средние концентрации ДДТ и его метаболитов у коренных родильниц по 4-м основным регионам Севера очень близки по величине: по сумме ДДТ – 1,7-2,7 мкг/л плазмы, по 4,4 ДДЕ – 1,4-2,4 мкг/л.
Процентный состав отдельных метаболитов ДДТ от суммы ДДТ в материнской крови (Табл. 3) примерно одинаков по северным регионам. Наибольший вклад в сумму ДДТ вносит самый устойчивый метаболит 4,4 ДДЕ – от 82% до 95%.
Отношение 4,4ДДЕ/4,4ДДТ, составляющее 5,5-9 для основных регионов, свидетельствует о факте относительно недавнего загрязнения (10-15% свежего 4,4 ДДТ), а отношение 14,4 на Камчатке, и особенно 22 на Арале – о значительности срока давности загрязнения (лишь 4-6% свежего 4,4 ДДТ).
Процент остальных нестойких метаболитов ничтожен (2,4 ДДЕ – не более 0,5%, за исключением Норильска, где уровни этого метаболита достигают 1,5%; 2,4 ДДД – сотые доли процента, за исключением Норильска и Камчатки, где уровни составляют соответственно 1 и 0,5%; 4,4 ДДД – не более 1,3%; 2,4 ДДТ – менее 2%).
Таблица 3.
Усредненный % метаболитов ДДТ от суммарной концентрации ДДТ в материнской крови по регионам.
мкг/л |
|
ЧАО конт. |
ЧАО прибр. |
Мурм. обл. |
НАО |
ТАО |
Норильск |
Арал |
Камчатка |
Всего |
n |
67 |
59 |
16 |
38 |
69 |
59 |
30 |
8 |
346 |
2,4 ДДЕ |
% от
? ДДТ |
0,13% |
0,30% |
0,02% |
0,42% |
0,53% |
1,55% |
0,03% |
0,51% |
0,52% |
4,4 ДДЕ |
% от
? ДДТ |
84,42% |
88,24% |
88,41% |
81,78% |
86,15% |
86,42% |
95,20% |
92,53% |
88,27% |
2,4 ДДД |
% от
? ДДТ |
0,05% |
0,03% |
0,02% |
0,04% |
0,04% |
1,07% |
0,06% |
0,51% |
0,27% |
4,4 ДДД |
% от
? ДДТ |
1,05% |
1,28% |
0,41% |
0,84% |
0,68% |
0,08% |
0,28% |
0,68% |
0,60% |
2,4 ДДТ |
% от
? ДДТ |
1,78% |
0,61% |
0,25% |
1,86% |
1,18% |
0,21% |
0,07% |
0,51% |
0,70% |
4,4 ДДТ |
% от
? ДДТ |
12,61% |
9,59% |
10,94% |
15,07% |
11,54% |
10,72% |
4,32% |
6,43% |
9,68% |
4,4 ДДЕ /4,4 ДДТ |
ratio |
6,70 |
9,20 |
8,08 |
5,43 |
7,47 |
8,06 |
22,05 |
14,39 |
9,12 |
 - наиболее высокие концентрации. - наиболее высокие концентрации.
Репродуктивное здоровье в связи с воздействием ДДТ
Анализ проявления эффектов воздействия отдельных метаболитов ДДТ (и их суммы) на здоровье матери и плода проводился на общем массиве базы данных, включавшем 346 записей. Попытка вычленить контрольные группы (Норильск и Арал) приводила к невозможности детектирования эффектов (как в опытной, так и в контрольных группах) вследствие снижения объема совокупности.
Анализ эффектов ДДТ производился по нескольким основным направлениям: сравнивались средние (геометрические) концентрации в группах с наличием и без анализируемого признака, в рамках последовательно нарастающих четырех дозовых диапазонов оценивалась дозо-эффективная зависимость, рассчитывался относительный риск возникновения неблагоприятных эффектов при воздействии поллютантов.
Из 346 родильниц, занесенных в базу данных, неблагоприятные исходы беременности имели:
• преждевременные роды (< 37 недель) – 41 женщина;
• низкий вес новорожденных (< 2500 г ) – 22;
• выкидыши – 36;
• мертворождения и врожденные пороки развития - 16;
Мертворождения и врожденные пороки развития плода объединены в единый анализируемый параметр по причине немногочисленности этих фатальных эффектов в исследуемой совокупности. Из 16 совместно анализируемых случаев - 13 случаев мертворождений и 3 врожденных порока развития.
• Менструальных статус женщин оценивался по следующим параметрам:
• Возраст начала месячных (< 13 лет; 13 лет и >);
• Продолжительность менструальных циклов (< 28 дней; 28 дней и >);
• Длительность кровотечения (< 4 дней; 4 дня и >);
• Спазмы и боли при месячных (наличие, отсутствие);
Отдельно оценивалось соотношение числа новорожденных мальчиков и девочек в группах матерей с различной дозовой нагрузкой поллютантов.
4.2.1. Неблагоприятные исходы беременности (НИБ).
Концентрации метаболитов ДДТ в крови родильниц, имевших неблагоприятные исходы беременности (НИБ), в сравнении с контролем (отсутствие НИБ) представлены в таблице 4 и на рисунке 1.
Таблица 4.
Сравнение концентраций (мкг/л) метаболитов ДДТ в плазме крови родильниц, имевших и не имевших неблагоприятные исходы беременности.
|
Беременность
< 37 недель |
Вес новорожденных
< 2500 г |
Выкидыши |
Мертворождения и врожденные пороки |
Отсутствие НИБ |
n |
41 (11,8%) |
22 (6,4%) |
36 (10,4%) |
16 (4,6%) |
296 (85,5%) |
|
сред. геом. |
макс |
P - value |
сред. геом. |
макс |
P - value |
сред. геом. |
макс |
P - value |
сред. геом. |
макс |
P - value |
сред. геом. |
макс |
2,4 ДДЕ |
0,02 |
0,15 |
> 0.05 |
0,01 |
0,12 |
< 0.05 |
0,01 |
0,10 |
< 0.05 |
0,0 2 |
0,0 9 |
> 0.05 |
0,02 |
0,22 |
4,4 ДДЕ |
1,94 |
9,5 7 |
> 0.05 |
1,65 |
12,00 |
> 0.05 |
2,0 7 |
19,65 |
> 0.05 |
2,57 |
19,65 |
> 0.05 |
2,19 |
20,76 |
2,4 ДДД |
0,02 |
0,28 |
> 0.05 |
0,0 1 |
0,01 |
< 0.01 |
0,0 1 |
0,09 |
> 0.05 |
0,01 |
0,09 |
> 0.05 |
0,01 |
0,32 |
4,4 ДДД |
0,0 3 |
0,30 |
> 0.05 |
0,03 |
0,18 |
> 0.05 |
0,0 2 |
0,18 |
> 0.05 |
0,03 |
0,19 |
> 0.05 |
0,02 |
0,50 |
2,4 ДДТ |
0,03 |
0,75 |
> 0.05 |
0,0 8 |
0,75 |
> 0.05 |
0,0 2 |
0,14 |
< 0.05 |
0,0 2 |
0,08 |
> 0.05 |
0,0 3 |
0,75 |
4,4 ДДТ |
0,20 |
1,42 |
> 0.05 |
0,2 1 |
1,42 |
> 0.05 |
0,2 1 |
6,27 |
> 0.05 |
0,29 |
6,27 |
> 0.05 |
0,22 |
3,66 |
сум ДДТ |
2,29 |
10,58 |
> 0.05 |
2,0 4 |
12,27 |
> 0.05 |
2,36 |
25,91 |
> 0.05 |
3,01 |
25,91 |
> 0.05 |
2,5 5 |
21,4 1 |
Рис. 1.
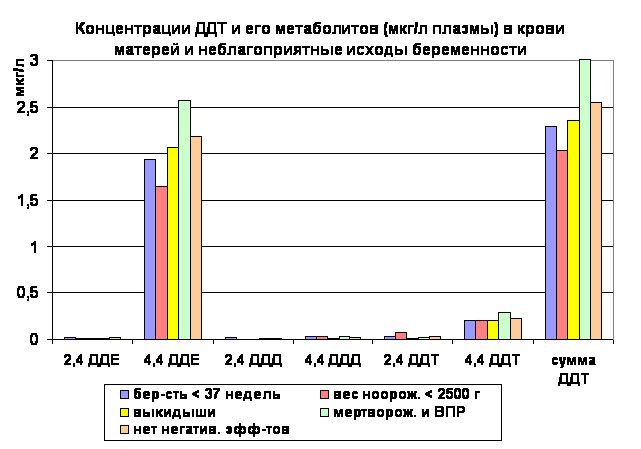
Очевидно, что концентрации таких метаболитов, как 2,4 ДДЕ, 2,4 ДДД, 4,4 ДДД и 2,4 ДДТ столь малы, что дальнейший анализ их возможного влияния на здоровье нецелесообразен. Остановимся на изучении двух основных метаболитов, концентрации которых в крови родильниц в 10-100 раз выше.
Рисунок 1 демонстрирует, что уровни 4,4 ДДЕ, 4,4 ДДТ и суммы ДДТ в крови женщин, имевших НИБ (включая недоношенность, низкий вес новорожденных и выкидыши), несколько ниже таковых у женщин, беременность которых протекала без патологии и потомство которых родилось здоровым, за исключением мертворождений и ВПР. При этом концентрации метаболитов ДДТ в крови женщин, имевших роды мертвым плодом и плодом с дефектами развития, хотя и были примерно на 20% выше, чем в контроле, но достоверных различий не наблюдалось.
Т.о., у женщин, имевших НИБ, не отмечено значимых различий в сравнении с контролем по средним уровням в крови ДДТ и его метаболитов.
Зависимость доза – эффект (в рамках последовательно нарастающих четырех дозовых диапазонов) для ДДТ приведена в Таблице 5.
Таблица 5.
Связь (дозовая зависимость) проявления неблагоприятных исходов беременности с концентрацией метаболитов ДДТ в материнской крови – приведены коэффициенты корреляции
|
Беременность короче 37 недель |
Вес
новорожденных менее 2500 г |
Выкидыши |
Мертворождения и врожденные пороки |
n (%) |
41 (11,8%) |
22 (6,4%) |
36 (10,4%) |
16 (4,6%) |
4,4 ДДЕ |
-0,31 |
-0,71 |
-0,50 |
0,14 |
4,4 ДДТ |
0,39 |
-0,33 |
-0,77 |
0,92 |
? ДДТ |
-0,62 |
-0,90 |
-0,85 |
0,20 |
- статистически значимая ( r > 0.7) связь эффекта с дозой.
Таблица 5 ясно показывает либо отсутствие зависимости НИБ от роста концентрации ДДТ и его основных метаболитов (r < 0.7), либо наличие отрицательной зависимости (r > 0.7), когда связь частоты проявления неблагоприятного эффекта с ростом дозы падает. Единственное исключение при данном подходе в анализе, - это тоже мертворождения и врожденные пороки развития плода. Однако данная форма патологии тесно позитивно связана лишь с ростом дозы 4,4 ДДТ, процентный вклад которого в сумму ДДТ невысок.
Т.о., увеличение концентрации в крови суммы ДДТ и его основного (на 80-90%) компонента 4,4 ДДЕ, не связано с увеличением частоты проявления неблагоприятных исходов беременности. Тесная положительная зависимость от роста дозы 4,4 ДДТ в крови матерей отмечена для мертворождений и врожденных пороков развития плода.
Расчетные показатели относительного риска возникновения неблагоприятных исходов беременности и патологии плода при воздействии ДДТ приведены в Таблице 6.
Таблица 6.
Относительный риск возникновения неблагоприятных исходов беременности и патологии плода при воздействии ДДТ
|
RR |
95% CI |
p-value |
4.4 ДДЕ (2,3 мкг/л плазмы крови родильниц) |
Беременность короче 37 недель |
0,80 |
0,41-1,55 |
0,51 |
Вес новорожденных менее 2500 г |
0,79 |
0,33-1,91 |
0,60 |
Выкидыши |
0,81 |
0,40-1,64 |
0,56 |
Мертворождения и врожденные пороки |
0,90 |
0,33-2,47 |
0,84 |
4.4 ДДТ (0,23 мкг/л плазмы крови родильниц) |
Беременность короче 37 недель |
0,81 |
0,42-1,55 |
0,52 |
Вес новорожденных менее 2500 г |
0,86 |
0,36-2,04 |
0,74 |
Выкидыши |
0,86 |
0,43-1,71 |
0,49 |
Мертворождения и врожденные пороки |
1,48 |
0,52-4,16 |
0,46 |
сумма ДДТ (2,5 мкг/л плазмы крови родильниц) |
Беременность короче 37 недель |
0,83 |
0,43-1,59 |
0,56 |
Вес новорожденных менее 2500 г |
0,80 |
0,34-1,91 |
0,62 |
Выкидыши |
0,76 |
0,38-1,52 |
0,44 |
Мертворождения и врожденные пороки |
1,67 |
0,59-4,69 |
0,33 |
Материалы таблицы 6 демонстрируют отсутствие повышенного относительного риска ( odd ' s ratio ) возникновения НИБ при превышении указанных уровней в крови ДДТ и его метаболитов, за исключением мертворождений и врожденных пороков развития плода, для которых величина риска превышает 1,5, при этом нижняя граница доверительных интервалов (95% CI ) и p - value свидетельствуют об отсутствии достоверности выявленных закономерностей.
4.2.2. Репродуктивный (менструальный) анамнез родильниц.
Каждый из параметров анамнеза анализировался попарно - при разбивке совокупности родильниц на две группы (Таблица 7, Рис. 2 и 3).
Таблица 7.
Концентрации (мкг/л) ДДТ и его метаболитов в плазме крови родильниц в сравниваемых группах с различными параметрами менструального статуса
Параметр анамнеза |
|
4,4 ДДЕ |
4,4 ДДТ |
сумма ДДТ |
месячные ранее 13 лет |
ср.геом. |
1,96 |
0,23 |
2,33 |
ср. ошибка |
0,20 |
0,03 |
0,22 |
t |
0,99 |
0,48 |
0,81 |
p-value |
> 0.05 |
> 0.05 |
> 0.05 |
n |
99 |
99 |
99 |
месячные с 13 лет и старше |
ср.геом. |
2,25 |
0,21 |
2,59 |
ср. ошибка |
0,21 |
0,03 |
0,22 |
n |
247 |
247 |
247 |
| |
|
|
|
|
менструальный цикл < 28 дней |
ср.геом. |
2,30 |
0,26 |
2,67 |
ср. ошибка |
0,34 |
0,09 |
0,42 |
t |
0,44 |
0,56 |
0,43 |
p-value |
> 0.05 |
> 0.05 |
> 0.05 |
| |
n |
68 |
68 |
68 |
менструальный цикл 28 дней и > |
ср.геом. |
2,13 |
0,21 |
2,47 |
ср. ошибка |
0,18 |
0,02 |
0,19 |
n |
278 |
278 |
278 |
| |
|
|
|
|
месячные до 4 дней |
ср.геом. |
2,10 |
0,16 |
2,36 |
ср. ошибка |
0,51 |
0,03 |
0,52 |
t |
0,15 |
0,87 |
0,34 |
p-value |
> 0.05 |
> 0.05 |
> 0.05 |
n |
61 |
61 |
61 |
месячные 4 дня и более |
ср.геом. |
2,18 |
0,23 |
2,55 |
ср. ошибка |
0,16 |
0,03 |
0,18 |
n |
285 |
285 |
285 |
| |
|
|
|
|
месячные с болями и спазмами |
ср.геом. |
2,50 |
0,23 |
2,89 |
ср. ошибка |
0,31 |
0,05 |
0,34 |
t |
1,62 |
0,32 |
1,68 |
p-value |
> 0.05 |
> 0.05 |
> 0.05 |
n |
146 |
146 |
146 |
месячные без боли и спазмов |
ср.геом. |
1,94 |
0,21 |
2,27 |
ср. ошибка |
0,15 |
0,02 |
0,16 |
n |
200 |
200 |
200 |
Рис.2
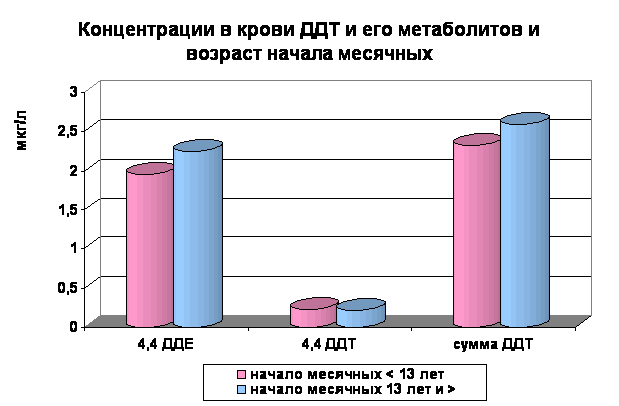
Рис.3
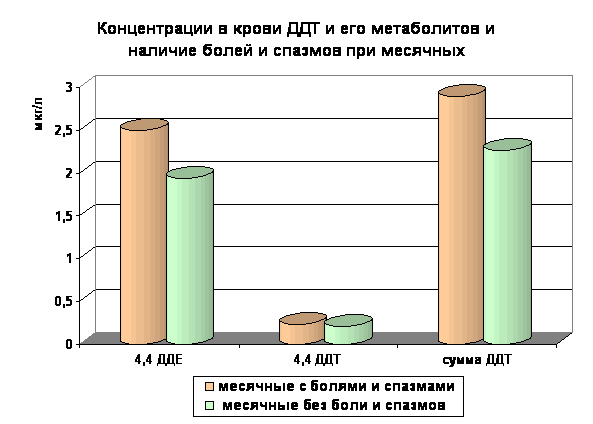
При рассмотрении таблицы 7 и рисунков 2 и 3, следует отметить, что ни по одному параметру менструального анамнеза (включая возраст начала месячных, продолжительность менструального цикла, длительность кровотечения, наличие болей и спазмов при месячных) достоверных различий в концентрациях в крови женщин, разбитых на парные группы, не выявлено. Женщины с болями и спазмами (при месячных) имеют более высокую концентрацию в крови ДДТ и его метаболитов, при этом достоверность различий более выражена, хотя не достигает необходимого уровня ( t < 2).
Зависимость доза – эффект (в рамках последовательно нарастающих четырех дозовых диапазонов) для ДДТ и его метаболитов приведена в таблице 8.
Таблица 8.
Связь параметров менструального статуса родильниц с концентрацией ДДТ и его метаболитов в крови – приведены коэффициенты корреляции.
|
Начало
месячных ранее 13 лет |
Месячные длительностью
< 4 дней |
Менструальный цикл < 28 дней |
Месячные с болями и спазмами
|
n (%) |
99 (28,6%) |
61 (17,6%) |
68 (19,7%) |
146 (40,3%) |
4,4 ДДЕ |
-0,50 |
0,11 |
0,25 |
0,93 |
4,4 ДДТ |
0,33 |
-0,38 |
0,86 |
0,28 |
? ДДТ |
-0,70 |
0,33 |
-0,12 |
0,99 |
- статистически значимая ( r > 0.7) связь эффекта с дозой.
Среди параметров менструального статуса родильниц повышение концентраций в крови ДДТ и его метаболитов не связано с длительностью месячных. Выявлена значимая корреляция суммы ДДТ с возрастом начала месячных – с ростом дозы месячные наступают позже. Рост дозы 4,4 ДДЕ и суммы ДДТ тесно коррелирует с увеличением числа женщин, имеющих при месячных боли и спазмы. Продолжительность менструального цикла значимо связана лишь с ростом дозы 4,4 ДДТ, процентный вклад которого в сумму ДДТ невысок.
4.2.3. Соотношение полов новорожденных детей.
Таблица 9.
Сравнение концентрации (мкг/л) ДДТ и его метаболитов в плазме крови женщин, родивших мальчиков и девочек.
Параметр анамнеза |
|
4,4 ДДЕ |
4,4 ДДТ |
сумма ДДТ |
мальчики |
ср.геом. |
2,12 |
0,22 |
2,46 |
ср. ошибка |
0,21 |
0,04 |
0,24 |
t |
0,26 |
0,16 |
0,32 |
p-value |
> 0.05 |
> 0.05 |
> 0.05 |
n |
187 |
187 |
187 |
девочки |
ср.геом. |
2,21 |
0,22 |
2,57 |
ср. ошибка |
0,24 |
0,02 |
0,25 |
n |
159 |
159 |
159 |
Рис. 4.
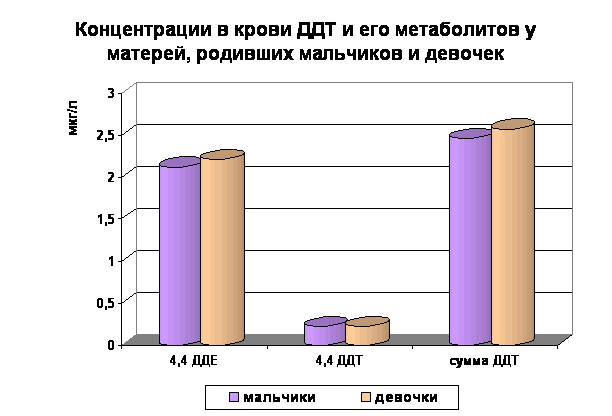
Таблица 9 и рисунок 4 демонстрирует отсутствие различий в концентрациях ДДТ и его метаболитов у женщин, родивших мальчиков и женщин, родивших девочек.
Выявить зависимость доза-эффект (влияние на изменение в соотношении полов новорожденных) в нарастающих дозовых диапазонах, не удалось (Рис. 5).
Рисунок 5.
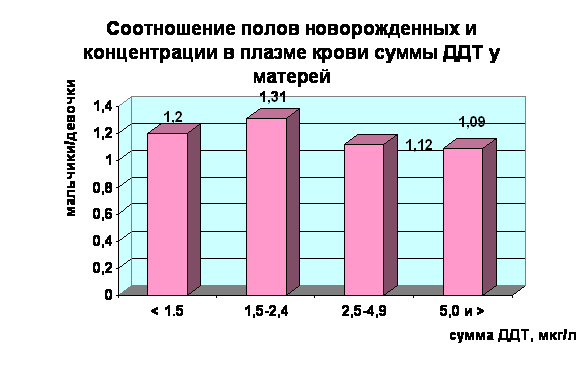
5. Выводы.
1. Уровни ДДТ в крови родильниц
Средние концентрации ДДТ и его метаболитов у коренных родильниц по 4-м основным регионам Севера РФ очень близки по величине: по сумме ДДТ – 1,7-2,7 мкг/л плазмы крови, по 4,4 ДДЕ – 1,4-2,4 мкг/л.
Максимальные персональные концентрации суммы ДДТ для изучаемых регионов достигали 8 мкг/л плазмы крови у родильниц коренных национальностей Российской Арктики, 26 мкг/л – у родильниц г. Норильск. При этом, вблизи г. Ургенч (приаральская зона экологического неблагополучия по пестицидам в Узбекистане) сумма ДДТ достигала 21 мкг/л плазмы крови родильниц-узбечек, что подтверждает явное присутствие местных источников ДДТ на Севере РФ.
Процентный состав отдельных метаболитов ДДТ от суммы ДДТ в материнской крови примерно одинаков по северным регионам. Наибольший вклад в сумму ДДТ вносит самый устойчивый метаболит 4,4 ДДЕ – от 82% до 95%.
Отношение 4,4ДДЕ/4,4ДДТ, составляющее 5,5-9 для основных северных регионов, свидетельствует о факте относительно недавнего загрязнения (10-15% 4,4 ДДТ от суммы ДДТ), а отношение 14,4 на Камчатке, и особенно 22 на Арале – о значительности срока давности загрязнения (4-6% 4,4 ДДТ).
2. Неблагоприятные исходы беременности (НИБ)
У женщин, имевших НИБ, не отмечено значимых различий в сравнении с контролем по средним уровням в крови ДДТ и его метаболитов. Уровни 4,4 ДДЕ, 4,4 ДДТ и суммы ДДТ в крови женщин, имевших НИБ (включая недоношенность, низкий вес новорожденных и выкидыши), были даже несколько ниже таковых у женщин, беременность которых протекала без патологии и потомство которых родилось здоровым, за исключением мертворождений и ВПР. Концентрации метаболитов ДДТ в крови женщин, имевших роды мертвым плодом и плодом с дефектами развития, хотя и были примерно на 20% выше, чем в контроле, но достоверных различий не наблюдалось.
Корреляционная связь частоты проявления НИБ с ростом дозы ДДТ и его метаболитов либо отсутствует (r < 0.7), либо отрицательна.
Не выявлено достоверного повышения относительного риска ( RR ) возникновения НИБ на уровне анализируемых концентраций в материнской крови ДДТ и его метаболитов.
3. Репродуктивный (менструальный) анамнез родильниц
Ни по одному параметру менструального анамнеза (включая возраст начала месячных, продолжительность менструального цикла, длительность кровотечения, наличие болей и спазмов при месячных) достоверных различий в концентрациях в крови женщин, разбитых на парные группы, не выявлено. Женщины с болями и спазмами (при месячных) имеют более высокую концентрацию в крови ДДТ и его метаболитов, при этом различия не достоверны.
Выявлена тесная корреляция роста дозы 4,4 ДДЕ и суммы ДДТ с увеличением числа женщин, имеющих при месячных боли и спазмы.
4. Соотношение полов новорожденных детей
Отсутствуют различия в средних концентрациях ДДТ и его метаболитов у женщин, родивших мальчиков и женщин, родивших девочек.
Не выявлена зависимость доза-эффект (влияние на изменение в соотношении полов новорожденных) в нарастающих дозовых диапазонах ДДТ и его метаболитов.
Итоговый вывод
Анализ имеющейся базы данных (346 родильниц, в основном – коренное население Севера РФ) не выявил достоверной связи частоты проявления неблагоприятных исходов беременности, изменения параметров менструального статуса, сдвига в соотношении полов новорожденных детей с концентрациями в плазме крови матерей ДДТ и его основных метаболитов 4,4 ДДЕ и 4,4 ДДТ в наблюдаемых диапазонах доз. При этом, численная ограниченность изучаемой когорты и относительно невысокие уровни доз не позволяют однозначно судить о причинно-следственных закономерностях нарушений здоровья.
Международный проект
по ликвидации СОЗ – IPEP
Website- www.ipen.org
|
|
| |
Центр
"Эко-Согласие" Для контактов:
Москва, 129090, а\я 43 tel: 7-095-924-62-40
fax:7-095-925-92-82 e-mail: accord@leadnet.ru |
|
